3.慗堏嬥懏尦慺傪娷傓峺慺偺婡擻
丂慗堏嬥懏僀僆儞傪曗峺慺傑偨偼曔寚暘巕懓偲偟偰娷傓偄傢備傞嬥懏峺慺偼懡條側婡擻傪帩偮偑丆偦偺偆偪摿偵廳梫側傕偺偼昞12-2偺傛偆偵惍棟偝傟傞丏

偙偙偱偼戙昞揑側椺偵偮偄偰働乕僗僗僞僨傿乕揑偵榖傪恑傔傞偑丆偙偺壢栚偺惈奿忋丆惗柦尰徾偺夝柧傛傝傕奺尦慺偺屄惈偑丆偄偐偵惗懱婡擻傪扴偆忋偵斀塮偝傟偰偄傞偐偵拝栚偡傞丏
乮暔幙戙幱傪彆偗傞峺慺偺椺偲偟偰丆嬻婥拞偺拏慺暘巕偐傜傾儞儌僯傾傪偮偔傞拏慺屌掕峺慺偲偟偰偺僯僩儘僎僫乕僛偑廳梫偱偁傞偑丆偙傟偼戞13夞偱埖偆.乯
乮侾乯垷墧峺慺偺壛悈暘夝怗攠
丂垷墧偼廃婜昞俀俹懓偺尦慺偱捠忢偼慗堏尦慺偵悢偊側偄偑丆惗暔柍婡壔妛暘栰偺廗姷偵廬偄堦墳懠偺慗堏尦慺偲偲傕偵榑偢傞偙偲偵偡傞丏
垷墧偼惗懱偵昁恵側尦慺偱偁傝丆偦偺僀僆儞傪娷傓嬥懏峺慺偱惈幙偺敾柧偟偰偄傞傕偺偼彮側偔偲傕廫悢庬偁傝丆Zn-僞儞敀幙寢崌偺夝棧掕悢乮埨掕搙掕悢偺媡悢乯偼10-10mol dm-3埲壓偲偝傟偰偄傞丏
垷墧嶖懱偺摿怓偲偟偰偼丆亄俀壙僀僆儞偑偐側傝崅偄揹壸枾搙傪傕偪丆偟偐傕亄俀壙偵屌掕偝傟偰偄傞偙偲丆攝埵悢偑係傑偨偼俇丆帪偵偼俆偲曄壔偟傗偡偄偙偲偑嫇偘傜傟傞丏
偙傟偼Zn2亄偺揹巕攝抲偑d10宆傪傕偮偙偲偵傛傞丏
垷墧僀僆儞偺栶妱偼儖僀僗巁偲偟偰婎幙偲憡屳嶌梡偟丆婎幙拞偺尨巕偙偲偵扽慺尨巕偺揹巕枾搙傪尭彮偝偣丆媮妀帋栻偺峌寕傪庴偗傗偡偔偡傞偙偲偵傛偭偰斀墳懍搙傪憹壛偝偣傞丏
偙偺傛偆側儖僀僗巁怗攠嶌梡偼嬒堦宯怗攠偺戙昞椺偱偁偭偰丆桳婡壔妛斀墳偵偼偟偽偟偽傒傜傟傞丏乮恾12-5乯
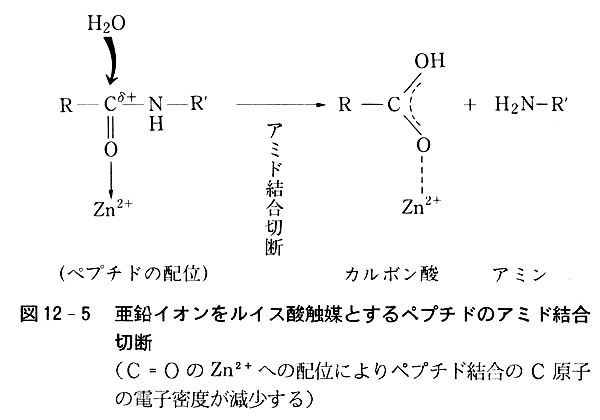
嬥懏峺慺偺懠偺晹埵偺栶妱偼婎幙偲偺暘巕娫憡屳嶌梡偵傛偭偰婎幙偲垷墧僀僆儞偲偺寢崌偑惗偠傗偡偄傛偆側忬嫷乮攝埵娐嫬偲傛傇乯傪嶌傞偙偲偵偁傞丏
丂戙昞椺偲偟偰恾12-6偵偼僇儖儃僉僔儁僾僠僟乕僛偺嶌梡傪愢柧偡傞堦偮偺峫偊曽傪柾幃揑偵帵偟偨丏
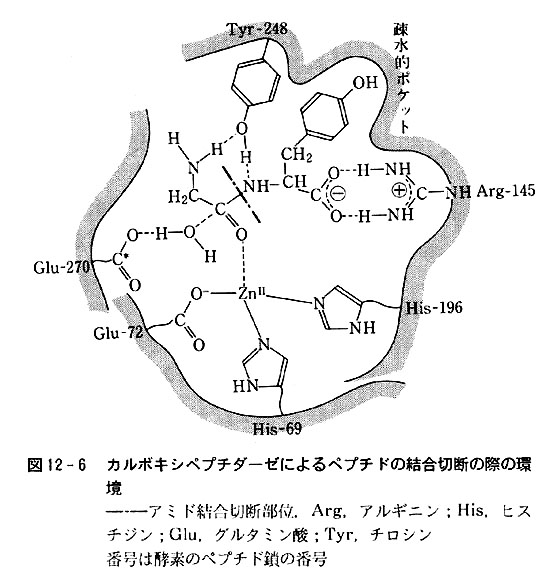
僇儖儃僉僔儁僾僠僟乕僛偼梉儞敀幙傗儁僾僠僪偺傾儈僪寢崌傪C-枛抂乮僇儖儃僉僔儖婎偑梀棧忬懺偵偁傞曽偺抂乯偐傜愗抐偡傞婡擻傪帩偮丏
偙偺拞偱Zn2亄僀僆儞偼傌僾僠僪嵔偺69斣媦傃196斣僸僗僠僕儞偺僀儈僟僝乕儖娐拏慺尨巕俀屄媦價72斣僌儖僞儈儞巁偺懁嵔僇儖儃儞巁僀僆儞偺巁慺尨巕偲寢崌偟偰偄傞丏
懡暘悈暘巕侾屄傕攝埵偟偰Zn2亄偼攝埵悢係傪帩偭偰偄傞丏
丂婎幙偺寢崌忬懺椺偲偟偰帵偟偨僌儕僔儖僠儘僔儞偼丆僠儘僔儞偺僇儖儃儞巁僀僆儞偑峺慺偺145斣傾儖僊僯儞偺傾儈僲婎偲丆僠儘僔儞偺傾儈僲婎偲僌儕僔儞偺傾儈僲婎偲偑248斣僠儘僔儞偺僼僃僲乕儖晹暘偲悈慺寢崌傪夘偟偰寢崌偡傞丏
傑偨僠儘僔儞偺朏崄娐偑峺慺偺慳悈惈晹埵偲憡屳嶌梡傪帩偮偙偲偵傛偭偰僌儕僔儖偺僇儖儃僯儖婎偑垷墧僀僆儞偵埨掕偵攝埵偡傞偺傪彆偗偰偄傞丏
壛悈暘夝傪惗偠傞悈暘巕偼270斣僌儖僞儈儞巁偺懁嵔僇儖儃儞巁僀僆儞偲寢傃晅偒丆Zn2亄僀僆儞偵寢崌偟偨僇儖儃僯儖婎偺扽慺尨巕偵嬤偯偄偰備偔丏
垷墧僀僆儞偑僇儖儃僯儖婎偺揹巕傪堷偒晅偗傞偺偱丆偙偺扽慺尨巕偺揹巕枾搙偼掅壓偟偰偍傝丆悈暘巕偺峌寕傪庴偗傗偡偔側偭偰偄傞傢偗偱偁傞丏
峺慺偺傌僾僠僪嵔偺怓乆偺傾儈僲巁巆婎偼婎幙偲垷墧僀僆儞偲偺寢崌傪彆偗偰偄傞丏
乮俀乯揹巕揱払嶌梡
丂懡偔偺僞儞敀幙偑偙偺婡擻傪扴偭偰偄傞偑丆偦偺惗柦婡擻偵壥偨偡栶妱偼抮偺壢栚偱怗傟傜傟傞婡夛偑懡偄丏
偙偙偱偼僞儞敀幙偺峔憿傗丆嬥懏僀僆儞偺壥偨偡栶妱偑柧傜偐偵偝傟偰偄傞椺偲偟偰丆僽儖乕摵僞儞敀傪庢傝忋偘傞丏
丂僽儖乕摵梉儞敀偼摵僀僆儞偲傌僾僠僪偐傜側傞暋崌梉儞敀幙偺憤徧偱丆600nm晅嬤偵嫮偄媧廂懷傪帩偪丆傑偨俤 俽 俼僗儁僋僩儖偵傕摿挜傪帩偮暋崌梉儞敀幙偱偁傞丏
侾暘巕拞偵摵尨巕嘥屄傪帩偮傕偺偲丆俀屄埲忋傪傕偮傕偺偲偁傝丆懡庬椶偺傕偺偑帺慠奅偵暘晍偟庬乆偺婡擻傪帵偡丏
恾12-7偵帵偡偺偼僷僙儕偺梩側偳偵娷傑傟傞僾儔僗僩僔傾僯儞偲偄偆僽儖乕摵僞儞敀偺堦庬偱丆暘巕検10,500傪傕偪丆梩墢懱偺拞偱揹巕揱払婡擻傪扴偆偙偲偑抦傜傟偰偄傞丏
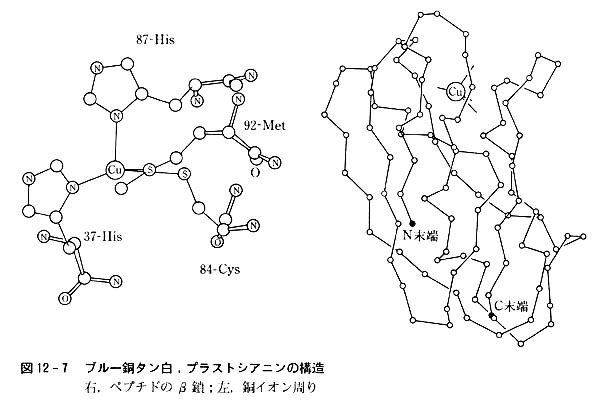
丂僆乕僗僩儔儕傾丒僔僪僯乕戝妛偺僼儕乕儅儞嫵庼偼梟塼忦審傪庬乆偵曄偊偨悈梟塼拞偐傜寢徎偝偣偨僾儔僗僩僔傾僯儞傪倃慄夞愜朄偱挷傋丆寢徎峔憿傪柧傜偐偵偟偨丏
侾暘巕拞偺傾儈僲巁巆婎悢偼99偱丆偄傢備傞兝嵔傪偮偔傝摵尨巕侾屄偑偦偺抂偺曽偵埵抲偡傞丏
拞惈梟塼偐傜摼偨寢徎偺摵廃傝偵偼37斣丆87斣偺僸僗僠僕儞偺僀儈僟僝乕儖拏慺尨巕丆84斣僔僗僥僀儞偍傛傃92斣儊僠僆僯儞偺棸墿尨巕偑攝埵偟丆備偑傫偩巐柺懱傪嶌偭偰偄傞丏
偙偺偲偒偺Cu-N媦傃Cu-S嫍棧偼昞12-3偵帵偡偲偍傝偱偁傞偑丆pH偑掅偄強偐傜摼傜傟偨寢徎拞偱偼87斣偺僀儈僟僝乕儖拏慺尨巕偵偼俫亄偑偮偄偰偄偰丆尨巕娫嫍棧傕戝偒偄丏
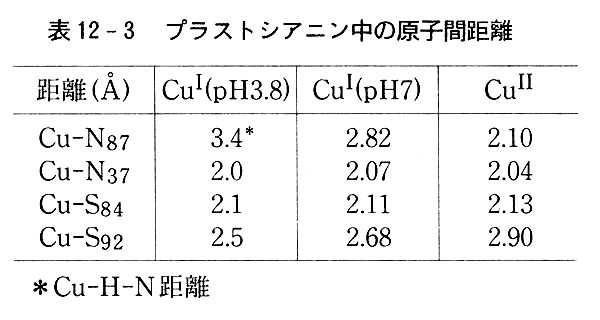
摵偑侾壙僀僆儞乮柍怓乯偐傜俀壙乮惵怓乯偵巁壔偝傟傞偲尨巕娫嫍棧偑尭彮偡傞偑丆婎杮揑側攝埵峔憿偼曄壔偟側偄丏
丂偙偺傛偆側曄壔偼寢徎峔憿夝愅寢壥偵婎偯偄偨暘巕柾宆偺塮憸偱傒傞偙偲偑偱偒傞丏
傑偨摵僀僆儞偺巁壔娨尦偵敽偆壜媡揑側怓偺曄壔偼幚尡偱傒傞偙偲偵偡傞丏
丂偙傟傑偱傒偰偒偨傛偆偵丆惗柦偵柍娭學偲傕傒側偝傟偨偙偲偺偁偭偨嬥懏尦慺壔崌暔偼丆懚嵼検偙偦彮側偄偑惗柦偵晄壜寚側婡擻傪扴偭偰偍傝丆偦偺帪奺尦慺偺屄惈傪斀塮偟偨嶖懱偺宍傪偲偭偰偄傞偙偲偑暘偐傞丏
偙偺傛偆側暘栰偼偛偔怴偟偔敪揥偟偰偒偨暘栰偱丆惗暔柍婡壔妛偲屇偽傟丆嶖懱壔妛偺廳梫側椞堟傪宍惉偟偮偮偁傞丏
丂
丂丂丂丂帒椏採嫙丂柤屆壆戝妛棟妛晹嫵庼丂嶳撪丂泫




