俁丏寢崌僄僱儖僊乕
丂壔妛寢崌偺嫮偝偼丆婎掙忬懺偵偁傞尨巕傪婎弨偲偟丆寢崌宍惉偵傛偭偰偳偺埵偺戝偒偝偺僄僱儖僊乕偑曻弌偝傟傞偐偵傛偭偰帵偝傟傞丅
偙傟偑寢崌僄僱儖僊乕偱偁傞丅
偙偺抣偼捠忢儌儖摉傝僉儘僕儏乕儖kJmol-1偱梌偊傜傟傞偑丆偦偺寢崌傪愗抐偟偰婎掙忬懺偺尨巕偵偡傞偺偵昁梫側僄僱儖僊乕偲峫偊偰傕傛偄丅
乮侾乯寢崌僄僱儖僊乕偺應掕
丂偙偺抣偼捈愙應掕弌棃傞偙偲偼彮側偔丆惗惉擬偺應掕偵婎偯偄偰娫愙偵媮傔傞丅
奺尦慺扨懱偺嵟傕埨掕側忬懺傪昗弨抣侽偲偟丆壔妛曄壔偵傛傝偁傞壔崌暔傪惗偠偨帪偵曻弌傑偨偼媧廂偝傟偨擬僄僱儖僊乕傪25亷侾婥埑偱偺抣偵姺嶼偟偨傕偺傪偦偺壔崌暔偺惗惉擬偲偄偆丅
扨懱偑侾婥埑25亷偱帩偮擬僄僱儖僊乕傪侽偲偡傞偺偼曋媂忋偱偁傞丅
偙偺偲偒媧擬傪惓偵丆曻擬傪晧偵偲傞丅
壔崌暔偺曐桳偡傞僄僱儖僊乕偺憹尭偲偟偰帵偡偨傔偱偁傞丅
丂侾婥埑25亷偵偍偗傞扨懱傪摨偠忦審壓偱偺婎掙忬懺尨巕偵曄偊傞偺偵昁梫側僄僱儖僊乕傕幚尡揑偵媮傔傜傟傞偑丆偦傟傜偼偡傋偰惓偺抣傪帩偮丅
婓僈僗尦慺埲奜偺扨懱偼婥懱偱傕屌懱寢徎偱傕丆尨巕娫偺寢崌偵傛偭偰偦傟偩偗埨掕壔偟偰偄傞傢偗偱偁傞丅乮昞2-5乯
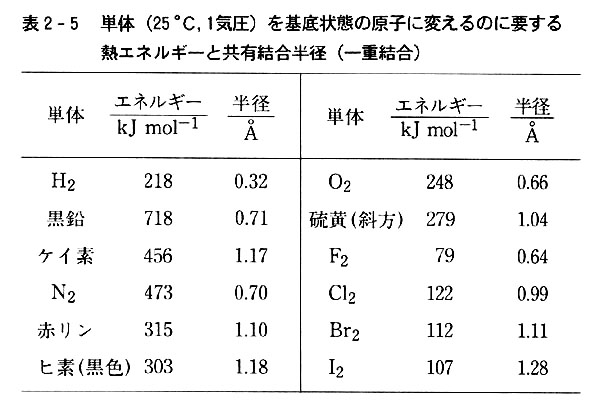
丂幚嵺偵俀庬埲忋偺扨懱偐傜壔崌暔傪惗偠傞帪偼暋嶨側壔妛斀墳傪宱桼偡傞偑丆偙偺帪扨懱偑偡傋偰堦扷婎掙忬懺偺尨巕偲側傝丆偦偺尨巕偐傜摉奩壔崌暔傪惗偠偨偲偟偰傕丆惗惉擬偼摨偠偼偢偱偁傞丅
偙偺偙偲偼僿僗偺朄懃偲偟偰抦傜傟偰偄傞偑丆傑偨僄僱儖僊乕晄柵懃偺堦偮偺尰傟偱傕偁傞丅
偡側傢偪恾2-5偺娭學偑惉棫偡傞丅
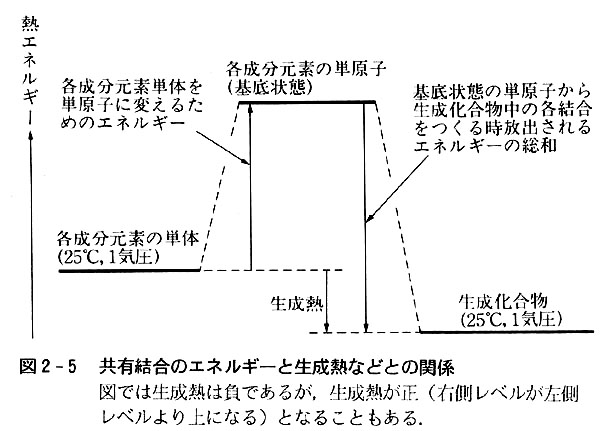
丂偙偺娭學傪梡偄傞偲丆應掕偝傟偨惗惉弉偲婎掙忬懺尨巕偺惗惉偵梫偡傞擬僄僱儖僊乕乮昞2-5乯偲偐傜丆壔崌暔拞偺尨巕娫偺寢崌僄僱儖僊乕偺憤榓偑媮傔傜傟傞丅
椺偊偽儊僞儞偺惗惉擬偼亅74.5kJmol-1偱偁傝丆偙傟偼侾婥埑25亷偺崟墧乮僌儔僼傽僀僩乯侾儌儖12.01倗偲丆摨忦審偺悈慺暘巕俀儌儖偐傜侾儌儖偺儊僞儞傪侾婥埑25亷偱嶌傞帪丆曻弌偝傟偨擬僄僱儖僊乕偵摉傞丅
堦曽丆摨検偺崟墧傪偡傋偰婎掙忬懺偺扽慺尨巕偲偡傞偺偵梫偡傞擬僄僱儖僊乕偼亄716.68kJmol-1丆俀儌儖偺悈慺暘巕傪係儌儖偺婎掙忬懺悈慺尨巕偵曄偊傞偵偼871.88kJmol-1傪梫偡傞丅
偙偺嵎堷偵傛偭偰C-H寢崌係屄偑惗偠偨偺偩偐傜丆僿僗偺朄懃偱師幃傪摼傞丅
丂4倶亖[亅74.5亅(716.68亄871.88)]乮扨埵kJmol-1乯
寁嶼偡傞偲倶亖415.9 kJmol-1偲側傞丅偙偙偱偺侾儌儖偼C-H寢崌偑傾儃僈僪儘悢偩偗偁傞偙偲傪堄枴偡傞丅
乮俀乯嫟桳寢崌僄僱儖僊乕偺堦斒抣
丂屄乆偺壔妛寢崌偺僄僱儖僊乕偼幚尡僨乕僞偐傜媮傔傜傟傞偑丆偦偺抣偼堦掕晄曄側傕偺偱偼側偔丆奺尨巕偑摉奩寢崌偺傎偐偵偳偆偄偆寢崌傪帩偮偐偵傛偭偰曄壔偡傞丅
椺偊偽C-H寢崌僄僱儖僊乕傕儊僞儞偲傋儞僛儞偲偱偼彮偟堘偆偟丆恷巁傗傾儖僐乕儖偱偼偝傜偵堎側傞丅
偦傟偱傕丆偁傞尨巕娫偺寢崌僄僱儖僊乕偺戝懱偺抣偼丆奺庬偺峫嶡偵嬌傔偰廳梫偱偁傞偐傜丆昞2-6偵帵偟偨丅昞傪棙梡偡傞帪偵偼崱弎傋偨拲堄傪朰傟偰偼側傜側偄丅
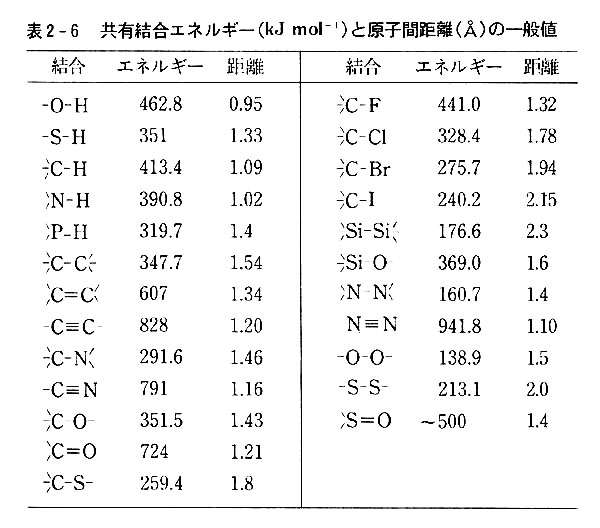
丂偙偺抣偼乽尒偐偗偺寢崌僄僱儖僊乕乿偲偄偆傋偒傕偺偱偁傞丅
嫟桳寢崌傪峫偊傞帪偵婎掙忬懺偐傜尨巕壙忬懺偵椼婲偟丆LCAO朄傪揔梡偡傞偙偲偑懡偄丅
婎掙忬懺偐傜寢崌忬懺偵堏傞帪偺擬僄僱儖僊乕偼丆尨巕壙忬懺傊偺椼婲僄僱儖僊乕乮媧擬乯偲尨巕壙忬懺偐傜寢崌忬懺偑惗傑傟傞帪偺曻弌僄僱儖僊乕偲偺嵎偵憡摉偡傞丅
乮俁乯寢崌僄僱儖僊乕偲尨巕娫嫍棧偲偺娭學
丂嫟桳寢崌傪嶌偭偰偄傞尨巕娫偺嫍棧偼惓妋偵應掕偝傟傞丅椺偊偽儊僞儞偺C-H偼1.0870侌乮倢侌亖10-10倣乯偱偁傞偑丆僄僞僲乕儖CH3CH2OH偺枛抂CH3婎偱偼1.09丆OH婎傪帩偮CH2忋偱偼1.10侌偱偁傞丅
奺尨巕偵寢崌偟偨懠尨巕偺庬椶偵傛偭偰抣偑曄壔偡傞丅
堦曽C-H忋偱偳偙傑偱偑C偺丆偳偙偐傜偑H偺椞堟偐傪寛掕偡傞偙偲偼崲擄偱偁傞丅
偟偐偟曋媂揑偵丆扽慺尨巕偺敿宎偼偙偺埵丆悈慺尨巕偱偼偙偺埵偲偄偆抣傪抦傞偙偲偼嬌傔偰桳塿偱偁傞丅
昞2-6偵偼奺尨巕娫偺嫍棧傪丆昞2-5偵偼嫟桳寢崌傪嶌傞敿宎傪梌偊偨丅
摨偠扽慺尨巕偱傕丆C-C偺帪偲丆C=C擇廳寢崌偺帪偲偱偼戝嵎偑偁傞丅
偙傟傜偺抣偼寢崌敿宎偲偄偆偺偑惓偟偄丅
尨巕偑僀僆儞偵側偭偨帪偺僀僆儞敿宎乮戞俉夞乯偼偝傜偵堎側偭偨抣偱偁傞丅
昞偱尒傞偲偍傝丆尨巕娫嫍棧偑抁偄傎偳寢崌僄僱儖僊乕偑憹壛偡傞偺偑堦斒懃偱偁傞丅
尨巕偺庬椶偵娭學側偔丆尨巕偳偆偟偑嬤偯偔掱尨巕娫偵偼嫮偄寢崌椡偑摥偒丆埨掕壔偡傞傢偗偱偁傞丅
丂丂丂丂丂丂帒椏採嫙丂暘巕壢妛尋媶強嫵庼丂淎揷丂塰帯


