戞俁復丂偄傠偄傠偺暘巕
丂暘巕偲偄偆尵梩偺堄枴傪彮偟峀偘傞偲丆乽堦掕悢偺尨巕偑寢崌偟偨廤抍偱丆侾屄偺撈棫偟偨棻巕偲偟偰峴摦偡傞暔乿偲掕媊偱偒傛偆丅
揹壸傪帩偮僀僆儞丆晄埨掕暘巕偱抁帪娫偟偐懚嵼偱偒側偄傕偺傕偙偺拞偵娷傑傟傞丅
傑偨嶖懱乮戞11夞乯暘巕偺拞偵偼尨巕悢偑悢廫偵媦傇傕偺傕偁傞丅
旕嬥懏尦慺偺嶌傞暘巕偺宍偼偄傠偄傠偱偁傞偑丆堦偮偺尨巕傪拞怱偵尒棫偰丆懠偺尨巕偼偦偺廃埻偵攝抲偝傟傞偲傒側偡偙偲偵傛偭偰宯摑揑偵棟夝偟傗偡偄丅
暘巕撪偱偺寢崌忬懺偼丆暘巕偺彅惈幙傪愢柧偟傗偡偄傛偆LCAO朄偱嬤帡偡傞丅
廳梫側暘巕偵偼悈慺壔暔丆僴儘僎儞壔暔丆巁壔暔側偳偺傎偐丆旕嬥懏尦慺偲巁慺偺尨巕偐傜側傞僆僉僜巁僀僆儞偑偁傞丅
扽慺偼懡庬椶偺桳婡暘巕傪梌偊傞偑丆拏慺偺棸壔暔丆儂僂慺偺奺庬壔崌暔偵傕撈摿偺傕偺偑偁傞丅
侾丏暘巕偺宍
乮侾乯暘巕宍偺暘椶
丂暘巕偺宍偼幚尡揑偵惛枾偵寛掕偱偒傞偑丆宍偑栤戣偲側傞偺偼俁尨巕暘巕埲忋偱偁傞丅
峔惉尨巕悢偺彮側偄応崌偼昞3-1偺傛偆偵惍棟偱偒傞丅
乮偙偺帪惓婯偺宍偐傜偺嬐偐偺偢傟偼柍帇偡傞丅椺偊偽丆墫壔儊僠儖CH3Cl偼惓妋偵偄偆偲C-Cl嫍棧偑C-H嫍棧傛傝傗傗挿偔丆乬惓乭巐柺懱偲偼偄偊側偄偑丆儊僞儞CH4偲摨偠惓巐柺懱偵暘椶偡傞丅乯
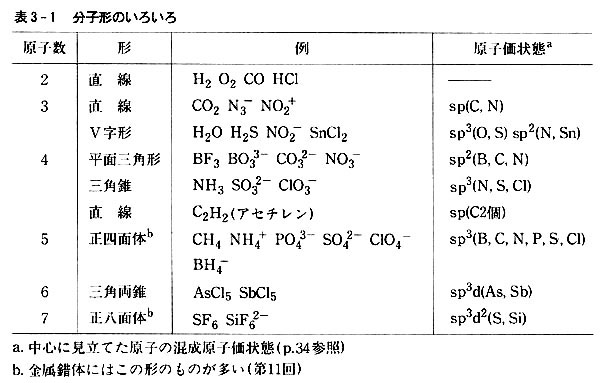
丂昞3-1傪棟夝偟傗偡偔偡傞偨傔偵丆捈慄宍側傜拞墰偺丆倁帤宆側傜捀揰偺丆嶰妏宍丆巐柺懱丆嶰妏椉悕丆敧柺懱側傜拞怱偵埵抲偡傞尨巕傪乽拞怱尨巕乿偲尒棫偰丆懠偺尨巕偼偦偺廃傝偵攝抲偝傟偨乽廃曈尨巕乿偲傒側偡丅
悈慺尨巕偼忢偵廃曈尨巕偱偁傝丆巁慺尨巕傕傎偲傫偳忢偵偦偆偱偁傞丅
僴儘僎儞尨巕偼巁慺尨巕傪憡庤偲偡傞帪埲奜偼傗偼傝廃曈尨巕偲側傞丅
棸墿偼帪偵廃曈尨巕偲側傞偙偲偑偁傞丅
懠偺尨巕偼傎傏椺奜側偔拞怱尨巕偵尒棫偰傜傟傞丅悈慺尨巕傪彍偔偲丆戝懱偵偍偄偰揹婥堿惈搙偺戝偒偄曽偺尨巕偑廃曈偵偔傞丅
乮俀乯揹巕懳斀敪懃偵傛傞愢柧
丂昞3-1偺宍偼偐側傝捈娤揑偵棟夝壜擻偱偁傞丅
拞怱尨巕偺廃傝偵偼廃曈尨巕偲偺寢崌揹巕懳偍傛傃寢崌偵娭梌偟側偄旕寢崌揹巕懳偑懚嵼偡傞偑丆偦傟傜揹巕懳偺岦偔曽岦偼憡屳斀敪偑嵟彫偵側傞曽岦偩偲峫偊傞丅
揹巕懳偼晧揹壸傪帩偮偐傜偙傟偼摉慠偱偁傞丅
揹巕懳偺悢偑俀,俁,係,俇偺帪偼偦傟偧傟捈慄丆惓嶰妏宍丆惓巐柺懱丆惓敧柺懱偺捀揰曽岦偵岦偔丅
俆偺帪偼巐妏悕偲嶰妏椉悕偺壜擻惈偑偁傞偑丆幚嵺偼傎偲傫偳偡傋偰屻幰偱偁傞丅
惓嶰妏宍偺捀揰偺堦偮偑旕寢崌揹巕懳偱愯傔傜傟傟偽丆暘巕宍偲偟偰偼倁帤宍偵側傞丅
丂拞怱尨巕廃傝偺揹巕懳悢偼師偺傛偆偵偟偰寛掕偝傟傞丅
乮兾寢崌乮p.48乯偑峫偊傜傟傞巁慺尨巕偑廃曈尨巕偲側傞応崌偼屻弎偡傞丅乯
廃曈尨巕偑悈慺傑偨偼僴儘僎儞尨巕偺帪偼偦傟傜偐傜奺侾屄偺揹巕偑寢崌懳宍惉偵嶲壛偡傞丅
拞怱尨巕偐傜偼庡検巕悢嵟戝偺揹巕婳摴偵偁傞揹巕偼偡傋偰寢崌懳傑偨偼旕寢崌懳宍惉偵娭梌偡傞丅
偙傟傜傪偡傋偰壛偊偨揹巕悢傪俀偱妱傞偲宍惉偝傟傞揹巕懳憤悢偑摼傜傟傞丅
偙傟偑忋婰偺傛偆側攝抲傪偲傞偲峫偊丆偦偺憡庤偲偟偰廃曈尨巕傪抲偔丅
憡庤尨巕偺側偄揹巕懳偼旕寢崌懳偵側傞丅
拞怱尨巕偐傜傒偰廃曈尨巕偑壗屄偐傪帵偡悢傪攝埵悢偲偄偆丅
乮偙偺尵梩偼婔壗妛揑側堄枴偱丆尨巕娫偺寢崌偺庬椶偼栤傢側偄丅乯
丂偙偺曽朄偼娙堈尨巕壙偵傛傞曽朄偲屇偽傟丆慹偄嬤帡偱偁傞偑丆峔憿偺傢偐偭偨暘巕偑偦偺宍傪偲傞棟桼傪愢柧偱偒傞偩偗偱側偔丆峔憿晄柧側暘巕偺戝懱偺宍傪悇掕偡傞偺偵傕栶棫偮丅
偨偩偟墳梡偱偒傞斖埻偼丆嵔傗娐傪嶌傜側偄斀帴惈暘巕偵尷傜傟傞丅
乮俁乯暘巕宍悇掕椺乮昞1-4丆p.21嶲徠乯
丂丂丂倎乯儊僞儞丂CH4丗拞怱尨巕C丆廃曈尨巕H丏
丂丂丂C偺嵟戝庡検巕悢俀傪帩偮揹巕係丆H係屄傛傝揹巕係丆揹巕懳傪嶌傞揹巕寁俉屄丆係懳丅
丂丂丂偦傟傜偺攝岦曽岦偼C偐傜惓巐柺懱偺捀揰曽岦丅H係屄偑愯傔傞丅
丂丂
丂丂丂倐乯傾儞儌僯傾丂NH3丗拞怱尨巕N丆廃曈尨巕H丏
丂丂丂N偺嵟戝庡検巕悢俀傪帩偮揹巕俆丆H俁屄傛傝揹巕俁丆揹巕懳傪嶌傞揹巕寁俉屄丆係懳丅攝岦曽岦偼N傪拞怱偲偡傞惓巐柺懱偺捀揰曽岦丅
丂丂丂偦偺偆偪俁屄偼H偱愯傔傜傟丆侾偮偼旕寢崌懳丅嶰妏悕宍丅
丂丂丂們乯榋僼僢壔棸墿丂SF6丗拞怱尨巕S丆廃曈尨巕F丏
丂丂丂S偺嵟戝庡検巕悢俁傪帩偮揹巕俇丆F俇屄傛傝揹巕俇丆揹巕懳傪偮偔傞揹巕寁12丆俇懳丅攝岦曽岦偼惓敧柺懱偺捀揰曽岦丅
丂丂丂F俇屄偑愯傔傞惓敧柺懱宍丅
丂丂丂巁慺尨巕偑廃曈尨巕偲側傞帪偼丆屻弎偺兾寢崌乮擇廳寢崌乯傪峫偊傞昁梫偑偁傝丆婔傜偐偺曗惓傪梫偡傞丅
丂丂丂婎杮揑峫偊偼兾寢崌偺懚嵼偵傛偭偰傕曄傢傜側偄丅
丂丂丂倓乯扽巁僀僆儞丂CO32-丗拞怱尨巕C丆廃曈尨巕O丏
丂丂丂屻弎恾3-4偺傛偆偵丆C偵=O侾屄丆-O亅俀屄偑寢崌偟偨偲傒側偡丅
丂丂丂俀屄偺-O亅偺寢崌偵娭梌偡傞揹巕偼奺侾屄偱偁傞丅
丂丂丂=O偼俀屄偺揹巕偑娭梌偟偆傞偺偱丆寢崌懳傪嶌傞揹巕憤悢偼係亄俀亄俀亖俉偲側傝丆係懳偑惗傑傟傞丅
丂丂丂偟偐偟侾懳偼慡懱偲偟偰偺暘巕宍偵偼塭嬁偟側偄兾寢崌傪嶌傞偺偱丆偙傟傪堦墳彍奜偟丆俁屄偺揹巕懳偑C偐傜傒偰惓嶰妏宍偺捀揰曽岦偵岦偔丅
丂丂丂偦偺偆偪俀屄偼-O亅偱丆侾屄偼=O偱愯傔傜傟傞丅
丂丂丂倕乯棸巁僀僆儞丂SO42-丗S(=O)2(-O亅)2偲彂偗傞偐傜扽巁僀僆儞偺応崌偲摨條丆S偐傜俇屄丆=O俀屄偐傜係屄丆-O亅俀屄偐傜俀屄丆寁12屄偑俇懳傪嶌傞偑丆兾寢崌梡偺俀懳傪彍偄偰係懳偑宍傪寛掕偡傞丅
丂丂丂偙傟傜偑惓巐柺懱偺捀揰曽岦傪岦偒丆惓巐柺懱宍暘巕傪嶌傝丆俀屄偼=O偱丆俀屄偼-O亅偱愯傔傜傟傞丅
乮係乯彫暘巕偺宍
旕嬥懏尦慺偺嶌傞暘巕偺懡偔偼丆捈慄丆惓嶰妏宍丆偍傛傃惓巐柺懱傪婎杮偲偟偨宍偱丆捀揰偺堦晹傪旕寢崌懳偑愯傔傞応崌傕偁傞丅
偡側傢偪攝埵悢偼係埲壓偺偙偲偑懡偄丅
攝埵悢偑俆埲忋偲側傞偺偼丆儕儞丆棸墿側偳廃婜昞偺戞俁廃婜埲屻偺尨巕偑拞怱尨巕偲側傞応崌偱丆偦偺帪偼3d婳摴偺揹巕偑崿惉尨巕壙忬懺偵嶲壛偡傞丅乮昞3-1乯
