2.電荷移動力と電導性有機物
特殊な分子の間にはファン・デル・ワールス力とは別の引力が働く。
その一つに電荷移動力がある。
この力はベンゼン環など共役二重結合を持つ分子に多くみられるが,顕著な色の変化を生じるだけでなく,電気的性質にも大きい変化をもたらす。
(1)電荷移動錯体
ヨウ素を色々の溶媒に溶かすと異なった色を生じることはかなり古くから知られていた。
ヨウ素蒸気は淡紫色であるが,四塩化炭素中では同色を示すのに,ベンゼン中では赤褐色になる。
可視・紫外部における電磁波吸収は分子中での電子の状態を反映しており(第1回),ベンゼン中で色の変化―つまり可視部での吸収の変化―はヨウ素分子自身に変化を生じたことを意味する。
無色のp-ヒドロキノンと淡黄色のp-ベンゾキノンを水溶液中で混合すると,濃緑色のキンヒドロンが沈澱する。
この時も色が顕著に変化しており,両分子の電子状態に変化のあったことを示す。(図4-1)
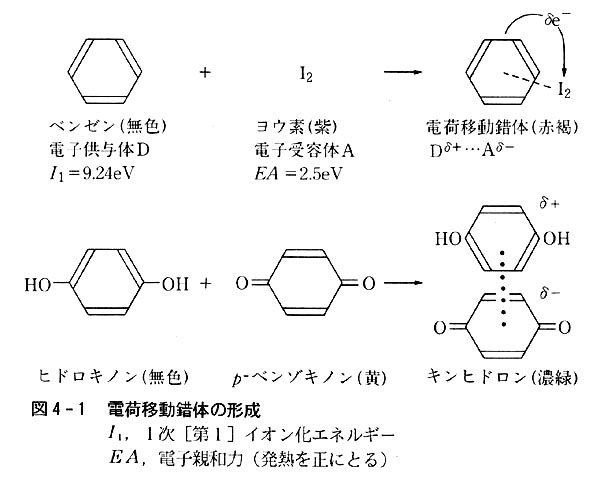
この反応も古くから知られ,キンヒドロンは電気化学的方法でpHを測定するのに用いられた。
これらの例では,分子がベンゼン環を持っていることが特色である。
べンゼン環では炭素原子上のπ電子が環と直角の方向で相互作用を持ち,共役二重結合を作っていることは第3回で学んだ。
このようなπ電子は比較的動きやすく,他の分子と相互作用しやすい。
ベンゼンのイオン化エネルギーが9.24eVと比較的小さいのもこの傾向を反映している。
ヨウ素のように電気陰性度の大きい
(電子を引き付けやすい,電子親和力2.5eV)
原子にあうとそちらに引っ張られて,ベンゼン環はやや正に,ヨウ素分子はやや負に帯電する。
ベンゼンの陽イオン,ヨウ素分子の陰イオンができるまでには到らないが,ややそれに近い状態になる。
この状態を示すのに,C6H6δ++I2δ-のような表現を用いる。
ここで生まれた電荷の偏りにより,ベンゼンとヨウ素の間には静電的引力が働くので安定な分子間化合物を生じるようになる。
キンヒドロンの場合も同様に電荷の偏りを生じ
C6H4(OH)2δ++C6H4O2δ-→{C6H4(OH)2・C6H4O2}
と表記されるような反応が起こっている。
このような変化では電荷が一方の分子から他方の分子に部分的に移動したと見ることができ,生じた一種の分子間化合物を電荷移動錯体という。
電子を与える側の分子(ベンゼン,ヒドロキノン等)を電子供与体,受け取る側の分子(ヨウ素,ベンゾキノン等)を電子受容体と呼ぶ。
(2)有機半導体・有機超電導体
分子が集まって生じた結晶―分子結晶―中では,電子は個々の分子に固定されており,分子間に移動することはない。
しかし電荷移動錯体の特殊なものになると,分子結晶中で電子がある程度自由に動くようになる。
この最初の例としては,1954年ペリレンC20H12と臭素の間の電荷移動錯体が室温で約8Ωcmという低い電気抵抗を示した。
その後種々の電荷移動錯体がさらに低い抵抗値を持つことが見いだされ,このような電導性を持った有機半導体(温度上昇と共に抵抗値減少)の研究は極めて盛んになった(図4-2,(a),(b))。
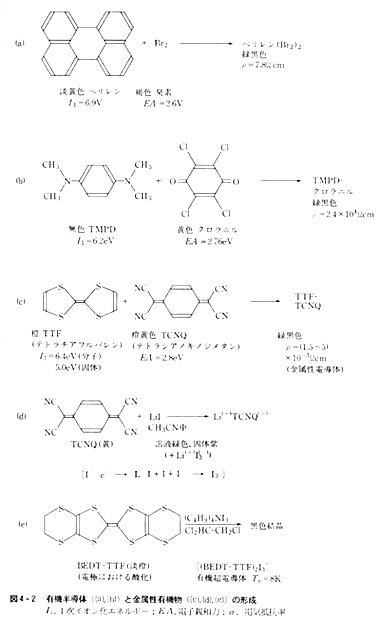
これらは単に学問的に興昧深いだけでなく,実用上も重要性を増しており,例えば反射型の複写機にも広く用いられている。
電荷移動錯体の中には金属性電導(温度上昇とともに抵抗値増加)を示すものがあり,有機金属体(organic metals)と呼ばれている。
(これは炭素原子と金属原子の間に直接結合を持つ有機金属化合物organometallic compound〔第13回〕とは全く別の物である。)
その中には電気抵抗値が室温で10-3~10-4Ωcmと,ビスマスなどの金属と同程度のものもある。
また低温において超電導を示すものさえ発見された。
超電導に移行する温度(超電導遷移温度)は10K程度であるが,金属と同様の現象を示す事実は極めて注目すべきものである。
これらの中には,電子受容体が完全に電子を失って1価陽イオンになった物もある。
(図4-2,(c),(d),(e))そのような電荷移動錯体は電気化学的な反応でも合成される。
一般に電荷移動錯体は濃い色を持つものが多いが,可視部から近赤外部に強い吸収帯が存在するためである。
くわしいことは映像によってみることにする。

