2.有機高分子の生成
炭素原子はそれ自身で長くつながった鎖状分子をつくるほか,他の原子を間に挟んで長くつながることもある。
単量体から高分子が生まれる時,水などの小さい分子が除かれることがある。
こういう重合反応を重縮合という。
これに対し,小分子を除くことなく重合が進行する反応を付加重合という。
(1)付加重合
テンプラの油を長い間使っていると,黒っぽくなって固まる傾向のあることはよく知られている。
これは植物油の分子中に二重結合(p.47)があり,その部分どうしで新しくC-C結合が生まれて分子が長くつながるためで,C-Cのπ結合が切れて,別な炭素原子との間にσ結合が生じる。
二重結合をもつ簡単な分子でもこのような反応が起こり分子が長くなる。

同じような反応がさらに続いて起こると,炭素原子が長くつながった鎖状分子ができる。
これが付加重合である。
炭素原子上に色々の側鎖をもつ単量体を原料として多くの高分子化合物がつくられ,実用化されている。
付加重合で生じた高分子化合物には直鎖または技分れした鎖状構造をもつものが多く,加熱すると成形しやすくなるため,熱可塑性樹脂と呼ばれ,押しだし,射出などの方法で加工される。
しかし,熱にあうと形が崩れたり,有機溶媒に弱いなどの欠点もある。
工業的に生産される高分子物質の80%は熱可塑性樹脂である。
付加重合は単量体を加熱したり光や放射線を照射しても起こるが,通常は触媒を用いる。触媒の種類によって重合反応の進行状況には差がある。
a. ラジカル重合 不対電子をもつ基が中間体となる反応で表6-2のように進行する。

触媒として-O-O-基をもつ過酸化物や,-N=N-結合をもつアジ化物を用いると,不対電子をもつラジカル(遊離基)を生じ,それが単量体の電子を引き抜いてラジカル-単量体結合をつくるとともに,単量体の末端に新たに不対電子を生み出し(成長末端という),それが単量体と反応して分子の鎖が伸びてゆく。
こうして単量体が長くつながった高分子を生じる。
次々と起こる反応を連鎖反応という。
ラジカルどうしが結合すれば鎖の伸びる反応は停止する。
熱や光で重合反応が開始される場合は,そのエネルギーで結合が切れてラジカルを生じ連鎖反応が進む。
ラジカル重合は1秒くらいの短時間に連鎖反応が進行するので,反応系の中には重合生成物と単量体が多く存在し,重合途中のものは少ない。
b. イオン重合 成長末端がイオンになって連鎖反応が進行するような重合をイオン重合という。
末端イオンが陽イオンの時はカチオン重合,陰イオンの時はアニオン重合という。
前者には硫酸など水素イオンを与えやすい酸や,BF3,AlCl3,TiCl4等のルイス酸(p.69),後者には塩基性の強いアルカリ金属やその水素化物,有機金属化合物などが触媒となる(表6-3)。

イオン重合は溶媒の種類によってかなり反応進行状況が異なる。
誘電率の小さい溶媒中では成長末瑞はイオン対(正負イオンが静電力で弱く結合したグループ)になっていて,そこへの単量体の付加が相手イオンの立体的規制を受けやすく,例えば側鎖Xが規則正しく一つおきに並ぶような立体特異的重合が起こりやすい。
誘電率の大きい溶媒では成長末端は遊離イオンになっているので,そのような規制は少ない。
しかし重合速度は大となりまた分子量の大きいものが生じやすい。
成長末端のアニオンは安定で,単量体がなくなっても残ることがある。(リビングポリマーという)
(2)重縮合
単量体どうしが反応する時に,2つの分子からそれぞれの一部が,小きい分子(多くは水)となって除かれる反応(縮合反応)で高分子化合物が生まれるのを重縮合(または縮合重合)という。
重縮合を起こす有機単量体分子は,-OH,-CHO,-COOH,-NH2などの官能基を2個以上もち,その部分の間で縮合反応を起こしてつながって行く。
その種類によって表6-4のような分類が可能である。

重縮合反応を進めるには温度を上げたり,圧力を低くして,除かれる分子を追い出すのがよい。
また逐次反応であるため,反応が進むほど平均重合度は高くなる。
数で示した平均重合度をPn,反応率をxとすると,
Pn=1/(1-x) (6.2)
の関係が成立し,x=0.99としてもPnは100に留まる。
またx→1につれて,Mw/Mn比は2に近づく。
重縮合で生じる高分子化合物には,タン白質(アミノ酸より),デンプン(グルコース),セルロース(グルコース)等鎖状に伸びた生体高分子のほか,ポリアミド(アミノ酸;ナイロン),ポリエステル(カルボン酸とアルコールまたはフェノール;テトロン)などの合成繊維,フェノール樹脂(フェノールとホルムアルデヒド),尿素樹脂(尿素とホルムアルデヒド)等の三次元に広がった網目状の結合を持つ合成樹脂がある。
重縮合で生じた高分子化合物でも,ポリアミドなど鎖状の分子からなるものは熱可塑性である。
しかし多価の酸と多価アルコール,ポリアミンとホルムアルデヒドなどの重縮合で生じたもので,官能基が完全に反応し終わっていない生成物は,熱を与えるとそれらがさらに反応して三次元構造がより密に形成され,硬くなるものもある。
これらは熱硬化性樹脂と呼ばれる。
フェノール樹脂,尿素樹脂,エポキシ樹脂などがこれで,耐熱性,耐溶媒性にすぐれているので,充填剤を加えて強靭な成形物をつくったり,強度の大きい繊維と組合わせて繊維強化プラスチックスなどの複合材料をつくる。
(3)高分子化合物中の化学結合
単量体が高分子化合物を造るさいの化学結合は通常の共有結合と変わらないのに,高分子化合物は低分子の場合とは異なった特性,例えば熱可塑性を示す。
長い鎖状構造をもつ熱可塑性高分子中では,-C-C-C-の鎖は絡み合っている。
これは個々の炭素原子周りに種々の立体配座(p.53)が可能なため,鎖が長くなるにしたがいとぐろを巻くような構造をとるからである。
その結果,きわめて多くの部分で分子間力が働く。
分子間の引力は分子内の結合力に比べれば著しく小さいが,作用点が多い場合は全体として無視できない力となる。
しかし分子内回転のエネルギー障壁は低いから(図3-6),温度が高くなると,C-C軸周りの回転は自由となり,変形しやすくなる。
共有結合のエネルギーはそれに参加する原子が当該結合の他にどういう結合をつくっているかによって変化することはp.39に述べた。
長い炭素原子鎖をもつ高分子化合物の場合,少しずつ異なった強さをもつ-C-C-結合が存在する可能性がある。
こういう状態を調べるための一つの有力な手段は,高分子のイオン化エネルギーを測定することである(p.22)。
(4)分子のイオン化エネルギーの測定
分子のイオン化エネルギーの多くは8~15eVであるが,これを測定するにはこれよりやや高いエネルギーをもつ電磁波を照射し,分子からたたき出されてくる電子(光電子という)のエネルギーを計るのがよい。
(照射エネルギー)-(出てきた電子のエネルギー)
=(分子のイオン化エネルギー) (6.3)
8eVのエネルギーは電磁波の波長に換算すると155nmとなる。
さらに高い結合エネルギーをもつ電子を取り出そうとすると,照射する電磁波としてはこれよりかなり短い波長の波が必要となる。
この波長はX線と紫外線の中間に当たり,光源が得にくい領域である。
この領域の光源として用いられるものにシンクロトロン軌道放射(SOR)がある(図6-1)。

これは光速度に近い速さで走っている電子が磁場によって曲げられると,接線の方向に電磁波を放射するという性質を利用したものである。
放射される電磁波は連続した波長をもつが,走っている電子のエネルギーが高いほど,最低波長は短い。
これを分光器に通して一定波長の電磁波を取り出して試料に放射し,出てきた電子のエネルギーと照射される方向を分析器を用いて測定する(図6-2)。
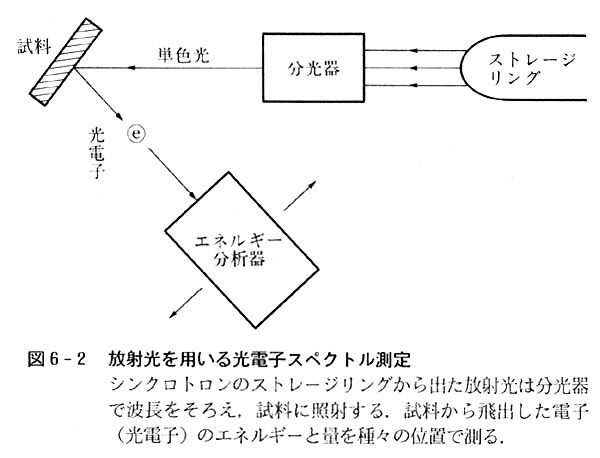
異なったイオン化エネルギーをもつ(異なる強さで分子に結び付けられている)電子が存在すると,式(6-3)を満足する色々なエネルギーの電子が観測される。これを光電子スペクトルという。
図6-3は52eV(波長24nm)でポリエチレン(-CH2-CH2-)nを照射したときの光電子スペクトルである。
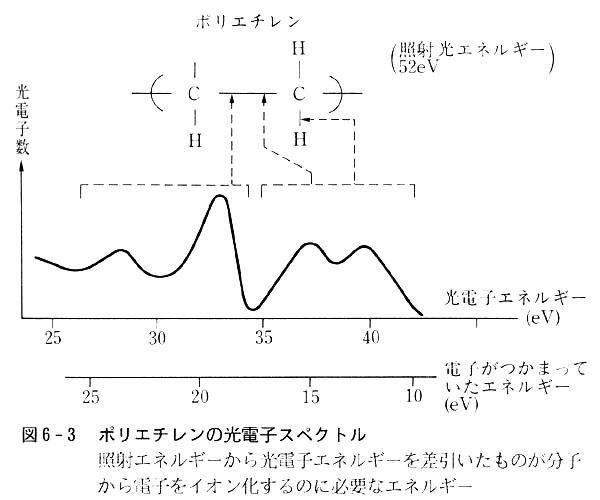
C-H結合とC-C結合では別のエネルギー領域に光電子を与える。また図6-4のように炭素原子数が増すにつれてC-C領域では色々のエネルギーをもつ電子が生じていることが分かる。
炭素原子数が10を超えて高分子に近づくと光電子スペクトルは連続となり,少しずつ違ったエネルギーで分子に結合している電子があることを示してある。
シンクロトロン放射光を発生する装置や,実験データは映像でくわしくみることにする。








