3丏惉憌寳僆僝儞
仠惉憌寳僆僝儞偺宍惉
丂戝婥拞偱僆僝儞偑惗惉偡傞偨傔偵偼巁慺尨巕偺惗惉偑昁梫偱偁傞丏
巁慺尨巕偼巁慺暘巕偲寢崌偟偰僆僝儞乮03乯傪惗惉偡傞偐傜偱偁傞丏
巁慺尨巕偼攇挿偑242nm傛傝抁偄巼奜岝偵傛傞巁慺暘巕偺岝暘夝偵傛傝惗惉偝傟傞乲斀墳乮13.1乯乴丏
巁慺尨巕偼巁慺暘巕偲嶰懱斀墳乮斀墳偺戞嶰懱丆M偼嬻婥暘巕乯偵傛傝僆僝儞傪惗惉偡傞乲斀墳乮13.2乯乴丏
惗惉偟偨僆僝儞偼庡偵350 nm傛傝傕抁攇挿偺懢梲偺巼奜岝傪媧廂偟偰岝暘夝偟嵞傃巁慺尨巕偲巁慺暘巕傪惗惉偡傞乲斀墳乮13.3乯乴丏
傑偨僆僝儞偼巁慺尨巕偲偺斀墳偵傛偭偰傕暘夝偟丆2屄偺巁慺暘巕傪惗惉偡傞乲斀墳乮13.4乯乴丏
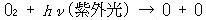 丂丂丂丂丂丂(13.1)
丂丂丂丂丂丂(13.1)
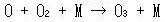 丂丂丂丂丂丂丂(13.2)
丂丂丂丂丂丂丂(13.2)
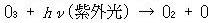 丂丂丂丂丂丂(13.3)
丂丂丂丂丂丂(13.3)
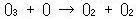 丂丂丂丂丂丂丂丂丂丂(13.4)
丂丂丂丂丂丂丂丂丂丂(13.4)
斀墳(13.1乯丆乮13.2乯偱惗惉偟偨僆僝儞偑斀墳乮13.3乯丆乮13.4乯偱徚柵偡傞偺偱惉憌寳僆僝儞偺崅搙暘晍偼斀墳乮13.1乯乣乮13.4乯偺僶儔儞僗偱寛傑傞丏
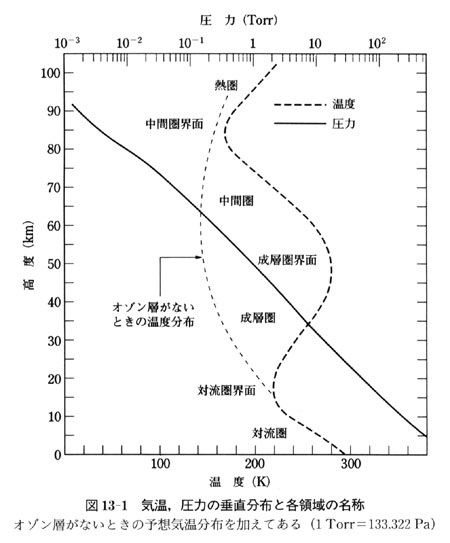
偡側傢偪丆僆僝儞偺惗惉棪偼懢梲巼奜岝偺嫮偝偲戝婥枾搙偺愊偵斾椺偡傞.恾13-2偵帵偡傛偆偵懢梲偺巼奜岝偼巁慺暘巕傗僆僝儞偵媧廂偝傟傞偺偱丆崅搙偑掅偔側傞傎偳尭悐偡傞丏
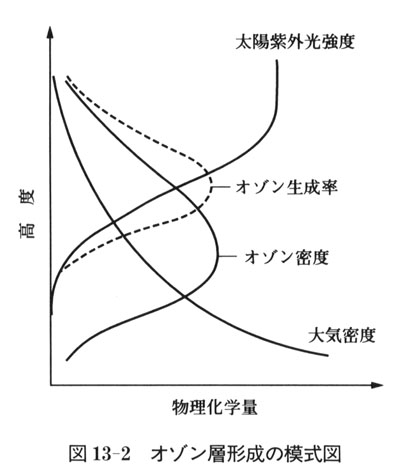
懠曽戝婥枾搙偼崅搙偑掅偄傎偳崅偄偺偱偙偺擇偮偺検偺愊偼偳偙偐偱嵟戝抣傪偲傞偙偲偵側傞乮恾13-2偺揰慄乯丏
幚嵺偺僆僝儞枾搙偺嵟戝抣偼偙偺傛偆偵偟偰媮傔偨崅搙傛傝丆偐側傝壓曽偵懚嵼偡傞偑丆偙傟偼戝婥偺塣摦偵傛傞傕偺偱丆惉憌寳偱偼僆僝儞偼壓曽偵岦偐偭偰塣偽傟偰偄傞丏
傑偨斀墳乮13.1乯乣乮13.4乯偼敪擬斀墳偱偁傞偨傔慡懱偲偟偰偼岝傪擬偵曄姺偟偰偍傝丆惉憌寳偵偍偗傞戝婥偺壏搙忋徃偑婲偙傞偺偱偁傞丏
仠惉憌寳僆僝儞偺幚應乮僆僝儞儗乕僓乕儗乕僟乕乯
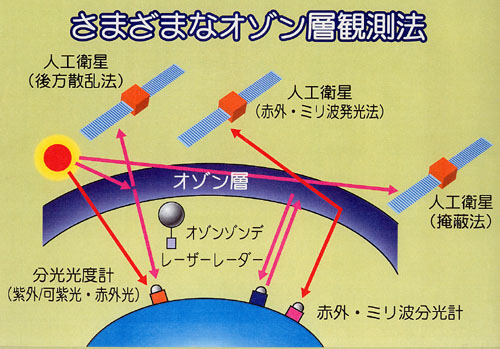
丂惉憌寳僆僝儞傪幚應偡傞曽朄偵偼恖岺塹惎傪梡偄偨庬乆偺暘岝應掕丆懢梲傪岝尮偲偟偨抧忋偱偺暘岝應掕側偳偺墦妘寁應朄丆偝傜偵偼僝儞僨偵寁婍傪搵嵹偟偰應掕偡傞曽朄側偳懡悢偺曽朄偑偁傞偑丆偙偙偱偼儗乕僓乕岝傪梡偄偨儗乕僓乕儗乕僟乕乮儔僀僟乕乯朄偵偮偄偰弎傋傞丏
僆僝儞儗乕僓乕儗乕僟乕偺尨棟偼恾13-3偵帵偟偰偁傞丏
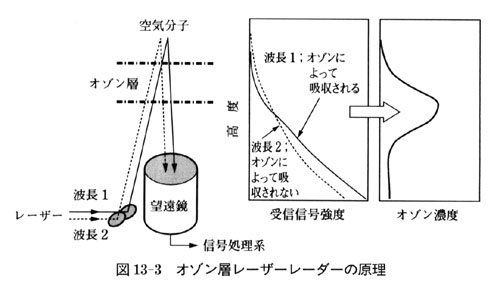
儗乕僓乕岝偼擇偮偺攇挿傪梡偄傞丏堦偮偼僆僝儞偵傛偭偰媧廂偝傟傞攇挿1乮308 nm乯丆傕偆堦偮偼僆僝儞偵傛偭偰媧廂偝傟側偄攇挿2乮355 nm乯偺岝偱丆偙偺2庬偺儗乕僓乕岝傪抧忋偐傜惉憌寳偵懪偪忋偘丆嬻婥暘巕乮N2偲O2乯偵傛傞嶶棎岝偺怣崋傪捈宎1.5 m偺朷墦嬀偱廤傔専弌偡傞丏
嶶棎岝偺嫮偝乮庴怣怣崋偺嫮搙乯偼掅崅搙偱嫮偔丆崅崅搙偱庛偄偑丆恾偵帵偡傛偆偵丆僆僝儞憌傪捠夁偟偰偒偨嶶棎岝偺崅搙暘晍偼攇挿侾偑僆僝儞偵傛傝媧廂偝傟傞偨傔堎側傞丏
攇挿1偲2偺嶶棎岝偺崅搙僾儘僼傿乕儖偺嵎偐傜僆僝儞擹搙偺崅搙暘晍偑媮傔傜傟傞丏
丂儗乕僓乕儗乕僟乕偵傛傞應掕偼抧忋10乣40 km偺僆僝儞憌娤應偵揔偟偰偍傝丆偦傟傛傝崅崅搙偱偼僆僝儞偐傜捈愙曻幩偝傟傞儈儕攇娤應偑梡偄傜傟丆10 km埲壓偺掅崅搙偱偼僶儖乕儞偵傛傞應掕偑峴傢傟偰偄傞丏
仠僼儘儞偵傛傞僆僝儞憌攋夡
丂旝検側婥懱偑戝婥拞偵偍偄偰戝偒側岠壥傪惗傓偵偼偦偺斀墳偑楢嵔斀墳偱偁傞偙偲偑昁梫偱偁傞丏
惉憌寳偵偍偗傞僆僝儞攋夡偺楢嵔斀墳偺戙昞椺偼埲壓偺嶰偮偱偁傞丏
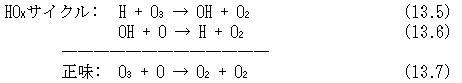
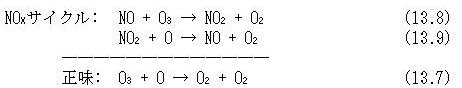
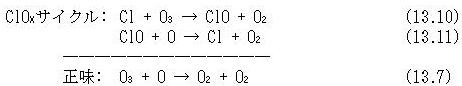
忋婰偺斀墳偵偍偄偰偼乮13.5乯偱偼悈慺尨巕丆乮13.8乯偱偼NO丆乮13.10乯偱偼墫慺尨巕偑斀墳偺奐巒偵娭梌偟丆偦傟傜偑斀墳偺廔傢傝偱偁傞乮13.6乯丆乮13.9乯丆乮13.11乯斀墳偵偍偄偰嵞惗偝傟傞揟宆揑側楢嵔斀墳偱偁傞丏
偙傟傜偺斀墳偵偍偄偰偼H丆OH丆NO丆NO2丆Cl丆ClO摍偺暘巕偼堦庬偺怗攠偲偟偰偺嶌梡傪偡傞偩偗偱丆悢検偵偍偄偰憹尭偑柍偔丆僆僝儞偺傒偑O2偵曄姺偝傟丆尭彮偟偰偄偔斀墳偱偁傞丏
HOX丆NOX僒僀僋儖偼忋婰偺斀墳偩偗偱側偔懠偵傕偄偔偮偐偺斀墳偑峫偊傜傟偰偄傞丏
惉憌寳偵偍偗傞悈慺尨巕傗NO偺僜乕僗偲偟偰偼偨偲偊偽丆埲壓偺岝暘夝斀墳偑偁傞丏
偙偙偱帵偡O(1D)偼捠忢偺巁慺尨巕傛傝僄僱儖僊乕偺崅偄椼婲巁慺尨巕偱偁傞丏
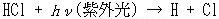 丂丂丂丂丂丂丂丂丂丂(13.12)
丂丂丂丂丂丂丂丂丂丂(13.12)
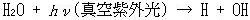 丂丂丂丂丂丂丂丂(13.13)
丂丂丂丂丂丂丂丂(13.13)
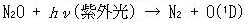 丂丂丂丂丂丂丂丂丂(13.14)
丂丂丂丂丂丂丂丂丂(13.14)
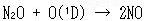 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂(13.15)
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂(13.15)
斀墳乮13.1O乯丆乮13.11乯偺ClOx僒僀僋儖偼1974擭偵暷崙偺壢妛幰儌儕乕僫乮M.J.Molina乯偲儘乕儔儞僪乮F.S.Rowland乯偑採埬偟偨斀墳偱丆惉憌寳偵僋儘儘僼儖僆儘僇乕儃儞乮CFC丆変偑崙偱偼僼儘儞偲屇傇乯偑怤擖偡傞偲懢梲偺巼奜慄偵傛傝CFC偑岝暘夝偟丆墫慺尨巕偑曻弌偝傟偰僆僝儞偑攋夡偝傟傞偲偄偆寈忇傪柭傜偟偨桳柤側斀墳偱偁傞丏
斵摍偼偙偺嬈愌偵傛傝丆1995擭搙偺僲乕儀儖壔妛徿傪庴徿偟偰偄傞丏
丂庬乆偺戝婥拞偺旝検婥懱乮偨偲偊偽CO2丆CH4丆N2O側偳乯偼嶻嬈妚柦埲屻媫寖偵憹壛偟懕偗偰偄傞丏
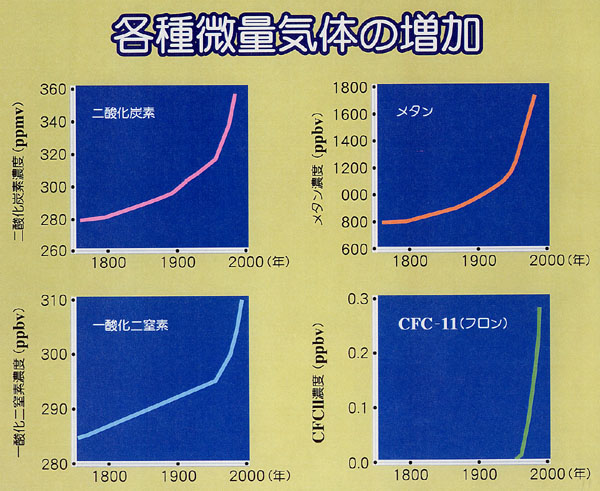
偲傝傢偗CFC偼戞擇師悽奅戝愴屻恖岺揑偵惢憿偝傟偨暔幙偱,夁嫀40擭娫偱戝婥拞偺擹搙偵偟偰僛儘偐傜悢昐ppt乮ppt偼10-12乯傑偱憹壛偟偨婥懱偱偁傞丏
仠僼儘儞偵傛傞僆僝儞攋夡偼幚嵺偵妋偐傔傜傟傞偺偐(岝壔妛僠儍儞僶乕幚尡)
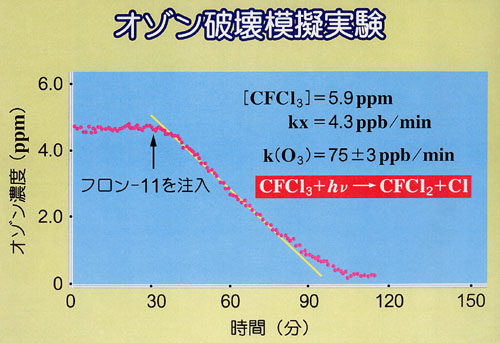
丂僼儘儞偺岝暘夝偵傛偭偰惗偠傞Cl尨巕偑幚嵺偵僆僝儞傪攋夡偡傞偐偳偆偐偺儌僨儖幚尡偺寢壥傪恾13-4偵帵偡丏
偙偺幚尡偼撪梕愊6 m3偺戝宆僠儍儞僶乕偵嬻婥傪1 / 10婥埑掱搙擖傟,惉憌寳偺懢梲岝偵嬤偄岝偱徠幩偡傞丏
僠儍儞僶乕撪偱乮13.1乯乣乮13.4乯偺斀墳偑婲偙傝丆乮13.1乯丆乮13丏2乯偱惗惉偟偨僆僝儞偑乮13.3乯丆乮13.4乯偱徚柵偡傞僶儔儞僗偵傛傝丆堦掕擹搙乮岝掕忢忬懺擹搙乯偺僆僝儞偑惗惉偡傞丏
偙偺忬懺偵CFC-11乮5.9 ppm乯傪壛偊傞偲栺1帪栤偱偡傋偰偺僆僝儞偼徚柵偟偰偟傑偆丏
偙偺偙偲偼CFC-11乮CFCl3乯偑岝暘夝偟丆曻弌偝傟偨Cl尨巕偑斀墳乮13.10乯丆乮13.11乯偺楢嵔斀墳傪婲偙偟偨偨傔偱偁傞丏
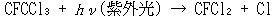 丂丂丂丂丂丂丂丂丂丂(13.16)
丂丂丂丂丂丂丂丂丂丂(13.16)
丂偙偺幚尡偱偼CFC-11偑5.9 ppm乮ppm偼10-6乯偲崅擹搙偱偁傞偨傔栺1帪娫偱偡傋偰偺僆僝儞偑徚柵偟偰偄傞偑尰幚偺惉憌寳戝婥偵偍偗傞CFC偺擹搙偼悢昐ppt偱偁傞偺偱斀墳偼傕偭偲備偭偔傝恑峴偡傞丏
仠尰幚偺惉憌寳僆僝儞尭彮偲懳嶔
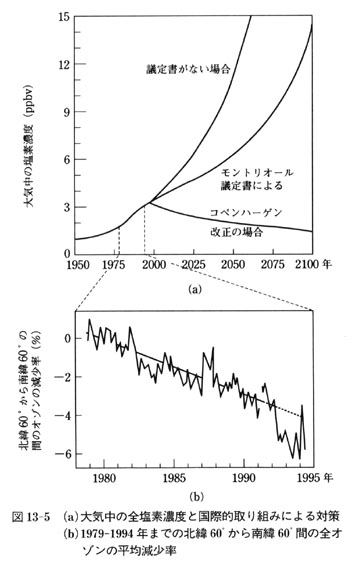
丂尰幚偺惉憌寳僆僝儞偑偳偺掱搙尭彮偟偰偄傞偐傪恾13-5乮b乯偵帵偡丏
恾13-5乮b乯偼杒堒60亱偐傜撿堒60亱傑偱偺娫偺撿杒拞堒搙娫偺忋嬻偵偁傞慡僆僝儞偑嵟嬤偺15擭娫偱偳傟偩偗曄壔偟偰偄傞偐傪帵偡傕偺偱偁傞丏
恾偐傜暘偐傞傛偆偵嵟嬤15擭偱偙偺椞堟偱偺慡僆僝儞偼5亾埲忋尭彮偟偰偄傞丏
偙偺僆僝儞偺尭彮偵懳偡傞懳嶔偲偟偰丆僼儘儞椶偺巊梡嶍尭傪惙傝崬傫偩儌儞僩儕僆乕儖媍掕彂偑1988擭偵敪岠偟丆偝傜偵1992擭偺僐儁儞僴乕僎儞偱偺戞巐夞掲栺崙夛媍偵偍偄偰僼儘儞丆僴儘儞丆巐墫壔扽慺丆僩儕僋儘儘僄僞儞摍偺巊梡傪1995擭枛傑偱偵慡攑偡傞偙偲偑寛掕偟偰偄傞丏
偙傟傜偺懳嶔偵傛傟偽恾13-5乮a乯偵帵偡傛偆偵戝婥拞偺慡墫慺擹搙偼棃悽婭屻敿偵偼僆僝儞儂乕儖弌尰埲慜偵栠傞偲婜懸偝傟丆偦傟偵傛偭偰丆惉憌寳僆僝儞偺尭彮偵傕帟巭傔偑偐偐傝丆僆僝儞憌偼尦偵夞暅偡傞傕偺偲婜懸偝傟偰偄傞丏
丂側偍丆扨埵柺愊摉傝偺悅捈嬻娫拰偵偁傞僆僝儞偺憤検傪昞偡抣偲偟偰僪僽僜儞偲偄偆扨埵偑傛偔巊傢傟傞丏
偙偺扨埵偼應掕偝傟偨cm2摉傝偺悅捈嬻娫拰偵偁傞僆僝儞悢傪2.687亊1016乮傾儃僈僪儘掕悢偺10-3攞乯偱妱偭偨抣偱偁傞丏
傕偆彮偟暘偐傝傗偡偔愢柧偡傞偲丆偙偺1 cm2摉傝偺悅捈嬻娫拰偵偁傞慡僆僝儞傪廤傔偰1婥埑偵偟偨偲偒偺岤傒傪10-3 cm傪扨埵偵偟偰昞偟偨傕偺偱偁傞乮300僪僽僜儞偺応崌姺嶼忋3 mm偲側傞乯丏
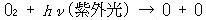 丂丂丂丂丂丂(13.1)
丂丂丂丂丂丂(13.1)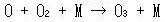 丂丂丂丂丂丂丂(13.2)
丂丂丂丂丂丂丂(13.2)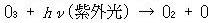 丂丂丂丂丂丂(13.3)
丂丂丂丂丂丂(13.3)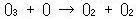 丂丂丂丂丂丂丂丂丂丂(13.4)
丂丂丂丂丂丂丂丂丂丂(13.4)


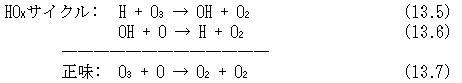
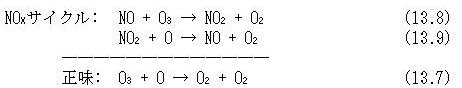
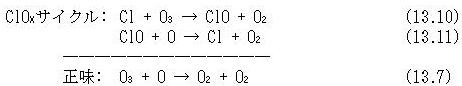
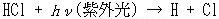 丂丂丂丂丂丂丂丂丂丂(13.12)
丂丂丂丂丂丂丂丂丂丂(13.12)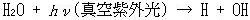 丂丂丂丂丂丂丂丂(13.13)
丂丂丂丂丂丂丂丂(13.13)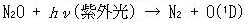 丂丂丂丂丂丂丂丂丂(13.14)
丂丂丂丂丂丂丂丂丂(13.14)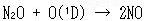 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂(13.15)
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂(13.15)

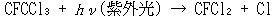 丂丂丂丂丂丂丂丂丂丂(13.16)
丂丂丂丂丂丂丂丂丂丂(13.16)
